安徽临床前动物实验公司
从微生物产物中发现和研制抗*****,是极其复杂的、综合性极强的工作,被称为“一条龙”,大致可分为五部分:①获得产生菌:从全国各地采集的土壤样本中,培养、分离数以千计的菌株。②制备发酵液样品:将各种各样的菌种进行培养发酵,取得为数众多的发酵液样品。③初筛检测:对大量的发酵液样品进行筛选,检出有潜在抗**活性的样品。④提取纯化:对初筛阳性发酵液样品中的有效物质,进行提取与纯化。⑤临床前动物实验疗效评价:利用实验动物**模型,观察提取物的疗效。化学药临床前动物实验指导原则;安徽临床前动物实验公司
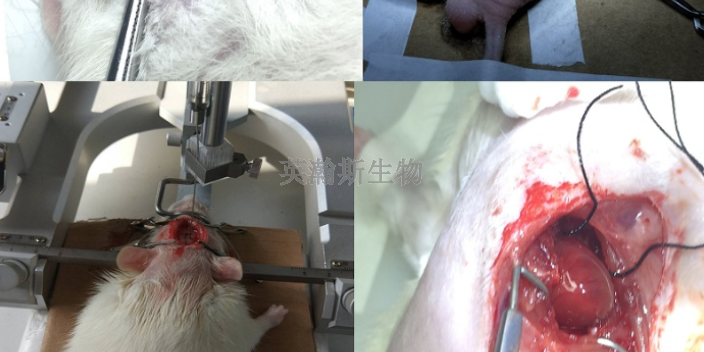
从临床前动物实验到临床试验,路在何方?这样的悲剧也揭示了一个令人不安的事实,人们对人类免疫系统的认识还存在很多盲点,而动物实验和临床试验也经常出现相左的结果。那么,我们现有的临床试验体系是否安全可靠?为了防止这样的悲剧再次发生,应该如何设计临床试验?从动物实验到人体试验,路该如何走?ESG根据调查结果并普遍征询了**意见后提出22条关于如何改善初次用于人体药物的Ⅰ期临床试验安全性建议。主要关注如何计算初次应用的药物剂量、如何给药;不同研究组织和医药公司应共享有关药物临床试验不良反应(特别是未发表的)、失败的药物试验等资料;特殊药物,例如作用于人体生理过程的生物药物,在进行研究之前应征求单独**的意见等。重庆值得信赖临床前动物实验是什么生物药临床前动物实验公司;
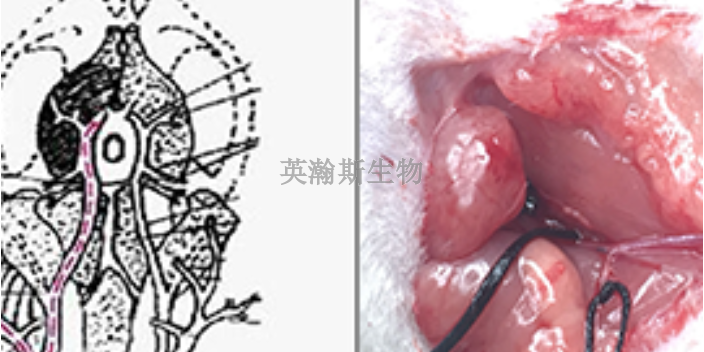
鉴于医疗器械创新发展迅猛和全球化发展趋势,实施医疗器械临床试验前安全性评价GLP管理是大势所趋。国家药品监督管理局医疗器械技术审评中心已经成立了医疗器械动物实验研究相关指导原则起草制定工作组,正在陆续发布针对具体类别的临床前动物实验研究相关指导原则。中国食品药品检定研究院医疗器械检定所初步搭建了医疗器械临床前动物实验研究平台。相信医疗器械动物实验研究领域会很快建立起健全的规范管理体系,为国内医疗器械的创新发展和百姓的用械安全保驾护航。
临床前动物实验模型选择的思路应遵循以下原则:一是要很大程度地模拟预期临床应用的实验系统,包括动物及其相关环境和生理特性。二是临床前动物实验研究实施的合理性,风险分析要素应涉及为什么选择该动物模型。如果动物模型有局限性,器械的一些相关风险比较好通过实验室或者尸体实验进行评价,并确定其相关性。除此之外,还应确定实验系统的遗传学差异(动物和人的差异)。如实验系统和人的不同、器械的尺寸和输送系统差异、器械植入的部位和追踪方式差异,等等。医疗器械临床试验前动物试验研究要点有哪些?

英瀚斯生物专做药品临床前动物实验。众所周知,人体试验的中心焦点之一是安全性,然而,安全性终究是相对的。为了减少人体试验的风险,在早期探索性研究中,临床前动物实验成为必经途径。模式动物的代谢类型、生理病理也能尽量与人类接近。动物实验从很大程度上帮助人类受试明显降低了风险,但不得不承认,动物实验和临床应用还是有很大差距的,动物实验的局限性无法通过自身去弥补。小白鼠是迄今比较成功、运用比较普遍的模式动物之一。然而,小白鼠的局限性也很明显。中国科学院遗传与发育研究所生物学研究中心高级工程师姜韬在接受《中国科学报》记者采访时就表示,作为实验动物的小白鼠毕竟不是灵长类而是啮齿目动物,代谢类型和生理病理在很多方面与人类差异甚大。化学药临床前动物实验是什么?北京临床前动物实验价格
中成药临床前动物实验公司;安徽临床前动物实验公司
临床前动物实验的计划和实验方案制定:首先,临床前动物实验研究必须经过周密计划。为此,实验计划需要有一定资质的机构或者个人提出,由有适当资质和经验的指定的专题负责人进行指导。专题负责人宜在实验场所办公,便于指导和监督实验技术的实施。专题负责人负责研究结果的解释、分析、形成文件和报告。实验方案应包括《药物非临床研究质量管理规范》第八章第二十九条中所要求的适用于一般GLP方案的十五项要素,并宜包含如特殊环境下的研究规范(操作指南)。任何**终已通过的实验方案的改变和修改以及修改原因都必须经由专题负责人签字并签署日期。实验方案和任何修改必须提供给质量保证部门检查。研究开始前需要先通过动物伦理委员会对已确定的实验方案进行审批。安徽临床前动物实验公司
上一篇: 四川有什么临床前动物实验机构
下一篇: 北京专注临床前动物实验机构