荧光pcr
在某些应用场景中,如实时定量PCR,较长的扩增产物可能不太适用,因为其扩增动力学可能较复杂,难以准确监测和定量。例如,在基因克隆中,如果需要克隆的基因片段较长,可能需要更细致地调整PCR反应条件以确保成功扩增;而在疾病诊断中,对于较短的特定标志物片段进行PCR扩增通常更容易实现准确快速的检测。在PCR反应中,过长的扩增产物可能会造成非特异性扩增,即产生与目标DNA不完全匹配的非特异性产物。这会增加反应体系的复杂性,降低PCR产物的纯度和特异性。因此,选择适当的扩增产物长度可以避免非特异性扩增,提高PCR产物的纯度。外参法是利用已知浓度的标准品来构建标准曲线。荧光pcr

在数据分析方面,需要正确选择合适的定量方法和内参基因。内参基因的选择要谨慎,以确保其在不同样本中的表达相对稳定。随着技术的不断发展,qPCR也在不断进化和创新。例如,数字PCR技术的出现,进一步提高了定量的精度和准确性。它通过将样本分割成无数个微小的反应单元,实现对单个DNA分子的定量分析。此外,与其他技术的结合也拓展了qPCR的应用范围。比如与微流控技术结合,可以实现高通量、自动化的qPCR分析,提高了实验效率。荧光定量pcr单位外参法将不同浓度的标准品进行实时荧光定量 PCR 反应,获得相应的 Ct 值,然后根据这些数据绘制标准曲线。
qPCR 广泛应用于基因表达分析。通过比较不同样本中特定基因的表达量,可以揭示基因在不同生理状态、发育阶段或疾病状态下的变化规律。这对于理解基因的功能和调控机制至关重要。研究人员可以深入探究基因与疾病的关联,为新药研发和策略的制定提供线索。qPCR 还在分子生物学的其他方面发挥着重要作用。比如,在遗传疾病的诊断中,它能够检测基因突变的存在和数量。对于一些遗传性疾病,如囊性纤维化、血友病等,通过 qPCR 可以准确地检测相关基因突变,实现早期诊断和遗传咨询。
探针的神奇之处还在于它可以标记不同波长的荧光基团,这为多重 PCR 反应的实现提供了可能。在多重 PCR 反应中,我们需要同时检测多个目标片段。如果没有合适的手段,这些目标片段的信号很容易相互混淆,难以分辨。而通过给不同的探针标记不同波长的荧光基团,我们就能够轻松地区分它们。每个标记了特定波长荧光基团的探针,就像是拥有了独特的“身份标识”。当它们与各自的目标片段结合并产生荧光信号时,我们可以根据不同的波长来准确地识别和区分这些信号。这就好比在一场盛大的音乐会中,每个乐器都发出独特的声音,我们可以清晰地分辨出小提琴的悠扬、钢琴的清脆等。循环阈值(Ct)是在 PCR 扩增过程中,荧光信号开始由本底进入指数增长阶段的拐点所对应的循环次数。
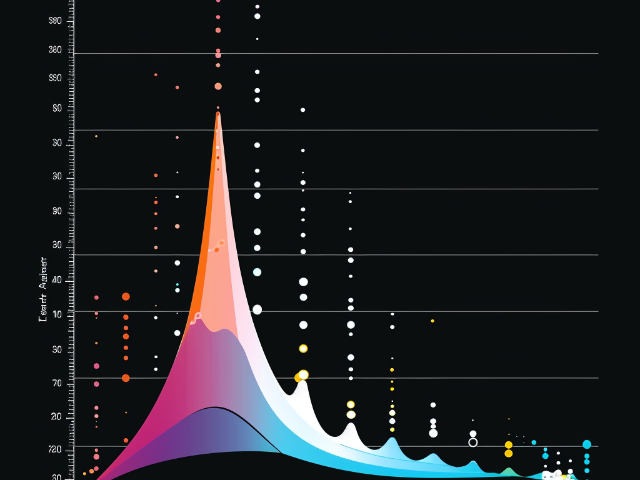
PCR产物熔解曲线图,简单来说,是通过监测DNA双链在逐渐升温过程中的解链行为而绘制出的曲线。其横坐标通常为温度,纵坐标为荧光信号的变化。这条曲线的形态和特征蕴含着丰富的意义。首先,它可以直观地反映出PCR产物的特异性。在理想情况下,一个纯净的、特异性的PCR产物会在特定温度下出现一个明显的熔解峰。这个峰所对应的温度就是该产物的熔解温度(Tm值)。如果产物中存在非特异性扩增或引物二聚体等杂质,曲线则可能会出现多个峰或异常的形状。由于Ct值与起始模板的对数存在线性关系,因此,实时荧光定量PCR是一种采用外标准曲线定量的方法。荧光pcr
在实时荧光定量PCR中,定量分析的关键在于根据荧光信号强度确定待测样品中特定DNA序列的数量。荧光pcr
实时荧光定量PCR技术基于传统PCR技术,但通过引入荧光标记和实时监测手段,实现了对PCR反应进程的动态跟踪和定量分析。在这个过程中,它不仅可以精细地捕捉到我们期望的特异性扩增产物,同时也能察觉到那些可能干扰实验结果的非特异反应产物。特异性扩增产物是实验的目标,它着特定基因或DNA片段的成功扩增。通过对这些产物的定量检测,可以获取关于目标基因表达水平、病原体载量等重要信息。实时荧光定量PCR技术利用荧光信号与扩增产物量之间的线性关系,能够高度准确地测量出特异性扩增产物的数量。荧光pcr